임재관 newsmedical@daum.net
식품의약품안전처(처장 이의경)가 ‘제네릭의약품 국제경쟁력 강화 민·관협의체’(이하 민관협의체)의 주요 논의과제를 공개하고, 6월까지 최종방안을 도출하기로 했다고 밝혔다.
민관협의체에서 앞으로 논의할 주요 과제는 다음과 같다.
◆생물학적동등성 시험 실시 제약사 표시 및 정보 공개 강화
제네릭의약품 중에서 생물학적동등성(이하 생동) 시험을 직접 실시하지 않고, 이미 실시한 업체에 위탁‧제조하는 묶음형 품목이 늘고 있어 제품에 실제 생동 제약사명 등을 표시하는 방안을 추진한다.
또 제조소 및 생동시험이 동일한 제네릭의약품에 대해 제조소 기준으로 하나로 묶어, 해당 정보를 식약처 홈페이지와 처방조제시스템 등을 통해 공개하는 방안도 고려중이다.
◆생동 품질평가 지표 개발, 평가 결과 공개
제네릭의약품의 품질 수준을 평가할 수 있도록 품질평가 지표를 마련하고, 평가 결과를 투명하게 공개해 제네릭의약품의 품질 수준과 신뢰도를 높여나간다는 계획이다.
또 전체 공정을 위탁해 제조하는 제네릭의약품은 위탁업체에도 품질관리 의무를 부여하고, 수탁업체의 품질관리를 엄격히 관리하도록 하는 등 위·수탁 간 책임관계를 명확히 한다는 방침이다.
◆성분별 제네릭의약품 데이터베이스 구축 추진
제네릭의약품의 글로벌 진출을 지원하기 위해 해외 바이어와 유통업체도 확인할 수 있도록 성분별 제네릭 현황을 영문화 하고, 세계보건기구(WHO)와 같은 국제기구에도 제공한다는 계획이다.
(표)제네릭의약품 동일제조소‘묶음형’품목 관리 예시
주성분 가바펜틴 경우, 2개 제조업체에 위탁하여 제조하는 품목이 5품목으로서 총 7품목이다.

식약처는 “이번 민관협의체에서 합의 진행 중인 내용이 정상 추진될 수 있도록 구체적인 제도개선 방안을 마련하고, 해당 제도개선 방안에 대한 자세한 실행계획을 6월 말까지 마련하고 발표할 계획이다”고 밝혔다.
한편 민관협의체는 지난 4월부터 제네릭의약품의 경쟁력 강화를 위해 제약업계‧학계‧의료전문가‧환자‧소비자단체 등 약 50명으로 구성‧운영 중이다.
제네릭의약품은 원개발의약품(오리지널)과 동등한 품질과 효능을 인정받아 오리지널의약품과 교체해 사용할 수 있는 의약품이다.
제네릭의약품의 동일제조소 묶음정보는 제네릭의약품에 대해 생동시험을 실시하고 직접 제조하는 품목과 이 품목에 위탁제조를 통해 품목허가를 받은 제품들을 하나로 묶어서 정리한 정보이다.
[메디컬월드뉴스]
- TAG



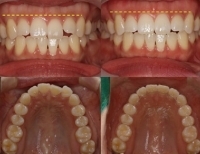 [치과에 대한 모든 것]일반적 치아교정과 앞니 미니교정의 차이점과 특징은?
[치과에 대한 모든 것]일반적 치아교정과 앞니 미니교정의 차이점과 특징은?
 앱 개발자 "인앱결제 가장 큰 문제는 과도한 수수료"
앱 개발자 "인앱결제 가장 큰 문제는 과도한 수수료"
 [성형외과 시술 제대로 알기]노화로 인한 얼굴 처짐 개선 ‘안면거상술’ 특징과 주의할 점은?
[성형외과 시술 제대로 알기]노화로 인한 얼굴 처짐 개선 ‘안면거상술’ 특징과 주의할 점은?
 5월 1일부터 병역미필자 모두에게 '10년 복수여권 발급'
5월 1일부터 병역미필자 모두에게 '10년 복수여권 발급'






