신개발 의료기기 시장 진입 최대 100일 단축…‘신의료기술평가-보험등재심사’ 동시 진행
‘의료기기 규제혁신 및 산업육성방안’ 후속조치
2019-07-04
임재관 newsmedical@daum.net
임재관 newsmedical@daum.net
앞으로 신개발 의료기기의 시장 진입 기간이 최대 100일 가량 단축될 것으로 기대된다.
보건복지부(장관 박능후)는 신의료기술평가-보험등재심사를 동시에 진행하는 내용의 ‘신의료기술평가에 관한 규칙’과 ‘국민건강보험 요양급여의 기준에 관한 규칙’ 개정안을 4일 공포‧시행한다고 밝혔다.
이번에 시행되는 ‘신의료기술평가-보험등재심사 동시 진행’은 지난 2018년 7월 발표된 ‘의료기기 규제혁신 및 산업육성방안’의 후속조치로 복잡한 규제절차로 인해 시장 진입이 다소 오래 걸렸던 부분(최대 490일)을 개선하기 위해 추진됐다.
이번 개정안이 시행됨에 따라 신의료기술평가와 보험등재심사의 동시 진행은 보험등재 심사를 신의료기술평가 기간 내에 진행시켜, 기존 순차 진행 시 발생했던 보험등재 심사기간(최대 100일) 만큼을 단축하게 된다.
(표)제도개선 전후 비교
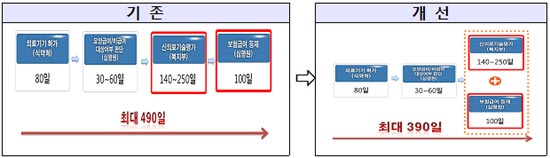
‘신의료기술평가-보험등재심사 동시 진행’ 절차를 신청하고자 하는 의료기기 업체 등은 신의료기술평가 신청 이후 최대 90일(체외진단검사 및 유전자 검사는 신의료기술평가 신청 시, 보험등재심사 자료 제출) 이내 보험등재심사에 필요한 비용 효과성 자료 등을 함께 구비해 한국보건의료연구원(원장 이영성)에 제출하면 된다.
복지부 손호준 의료자원정책과장은 “신의료기술평가와 보험급여 등재심사가 동시에 진행됨에 따라 그간 시장 진입이 길어져 발생했던 의료기기 업체의 어려움을 상당 부분 해소할 것이다”고 밝혔다.
[메디컬월드뉴스]



 [치과에 대한 모든 것]일반적 치아교정과 앞니 미니교정의 차이점과 특징은?
[치과에 대한 모든 것]일반적 치아교정과 앞니 미니교정의 차이점과 특징은?
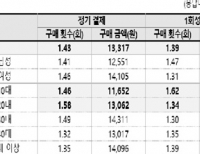 앱 개발자 "인앱결제 가장 큰 문제는 과도한 수수료"
앱 개발자 "인앱결제 가장 큰 문제는 과도한 수수료"
 [성형외과 시술 제대로 알기]노화로 인한 얼굴 처짐 개선 ‘안면거상술’ 특징과 주의할 점은?
[성형외과 시술 제대로 알기]노화로 인한 얼굴 처짐 개선 ‘안면거상술’ 특징과 주의할 점은?
 5월 1일부터 병역미필자 모두에게 '10년 복수여권 발급'
5월 1일부터 병역미필자 모두에게 '10년 복수여권 발급'






