김영신 medicalkorea1@daum.net
의료기기 주요 이모저모는 다음과 같다.
◆메드트로닉 약물 방출 풍선 카테터, 말기 신장질환 투석혈관 치료로 보험급여 확대
메드트로닉 ‘인팩트 약물 방출 풍선 카테터*(IN.PACT AV DCB, 이하 ‘인팩트 DCB’)’가 5월부터 폐쇄성 병변을 가진 만성 신부전 환자의 투석혈관 치료에 사용될 수 있게 됐다.
일반 풍선 카테터로 경피적 풍선혈관성형술을 받은 후 3개월 내 동정맥루에 재협착이 나타난 경우 보험급여를 받을 수 있다.
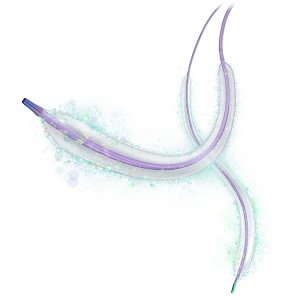
이번 인팩트 DCB의 적응증 확대 및 건강보험 등재로, 3개월 이내 동정맥루에 재협착이 나타난 환자들은 이제 인팩트 DCB로 투석 혈관을 관리할 수 있게 됐다.
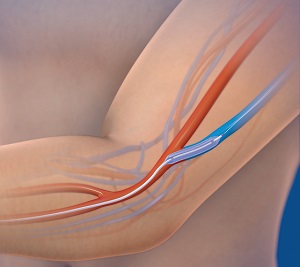
메드트로닉코리아 유승록 대표이사는 “이번 인팩트 DCB의 적응증 확대 및 보험급여로 국내 말기 신장질환 환자들의 고통을 덜어줄 혁신적인 치료 옵션을 제공할 수 있게 돼 자랑스럽다”며, “메드트로닉은 인팩트 DCB의 신속한 국내 임상 현장 도입을 통해 보다 안정적인 투석 치료 환경을 조성하는 데에 기여하겠다”고 밝혔다.
◆젠큐릭스, 액체생검 유방암 ESR1 돌연변이 진단제품 높은 정확도 입증
젠큐릭스 디지털 PCR 기반 드롭플렉스 ESR1 Mutation Test v2가 독일 다기관 연구에서 고감도 차세대염기서열분석 기반 진단기술과의 비교검증을 통해 96.8%의 높은 일치율을 보이며 뛰어난 신뢰성을 입증했다.
이번 연구는 독일의 샤리테 대학병원과 함부르크 병리학연구소 등에서 약 6,000건의 실 유방암 환자 데이터를 기반으로 진행됐으며, 32명의 환자 혈장 순환유리 DNA 샘플을 분석한 결과, 드롭플렉스 제품이 변이 대립유전자 비율이 약 0.5% 수준인 저빈도 돌연변이도 안정적으로 검출할 수 있음을 확인했다.
젠큐릭스의 드롭플렉스 ESR1 Mutation Test는 유럽 체외진단기기 인증을 획득했으며, 현재 독일을 시작으로 유럽 시장에서 실제 임상 현장에서 활용되고 있다.
◆코렌텍, 무릎 인공관절 ‘UCR 타입’ 美 FDA 승인 완료
코렌텍 무릎 인공관절 제품군인 EXULT Knee System의 새로운 삽입물 제품인 UCR 타입에 대해 미국 식품의약국(FDA)의 승인을 획득했다.
이번 FDA 승인을 받은 UCR 타입은 기존 제품의 한계를 극복하고, 외과의사가 후방십자 인대를 절제하거나 유지하는 수술 방식 모두에 적용이 가능한 제품으로, 수술 기법의 다양성과 환자 맞춤형 치료 옵션을 크게 확대할 수 있게 됐다.
코렌텍은 UCR 타입 출시 이후 2025년에 약 605만 달러, 2026년에는 약 786만 달러, 2027년에는 1,000만 달러 이상의 매출을 예상하고 있다.
◆GE 헬스케어, 헬스케어 아시아 메드테크 어워드에서 2관왕
GE 헬스케어는 찰튼 미디어 그룹이 주최하는 ‘헬스케어 아시아 메드테크 어워드 2025’에서 심장 관련 기술 혁신상 및 올해의 직원 참여상을 수상했다.
심장 관련 기술 혁신상은 GE헬스케어의 차세대 심장 MRI 기술인 소닉 DL™이 차지했다.
소닉 DL™은 FDA 승인을 받은 MRI 딥러닝 기술로, 단 한 번의 심장 박동으로 고품질의 심장 MRI 영상을 생성하며, 기존 방식보다 최대 83%(최대 12배) 빠른 검사가 가능하다.
특히, 이 기술은 심혈관 질환으로 매년 400만 명이 사망하는 아세안 지역에서 심장 질환 치료의 판도를 바꿀 기술로 기대받고 있다.
방사선 노출이 없는 비침습적 기술이라는 점에서 차별성을 가지며, 태아 심장 영상을 더욱 선명하게 촬영할 수 있도록 지원한다.
[메디컬월드뉴스 김영신 기자]



 [정형외과 시술 바로알기]장시간 컴퓨터·스마트폰 사용 ‘손목 결절종’ 원인부터 관리까지
[정형외과 시술 바로알기]장시간 컴퓨터·스마트폰 사용 ‘손목 결절종’ 원인부터 관리까지
 [모발이식 제대로 알기]합리적인 모발이식 ‘절개’ VS ‘비절개’…맞춤형 접근 중요
[모발이식 제대로 알기]합리적인 모발이식 ‘절개’ VS ‘비절개’…맞춤형 접근 중요
 [치과에 대한 모든 것]임플란트, 정밀 진단과 맞춤형 접근이 성공률 높여
[치과에 대한 모든 것]임플란트, 정밀 진단과 맞춤형 접근이 성공률 높여
 [정형외과에 대한 모든 것]러닝 인구 급증 속 건강 위해 ‘무릎·발목’ 관리도 필수
[정형외과에 대한 모든 것]러닝 인구 급증 속 건강 위해 ‘무릎·발목’ 관리도 필수
 [치과에 대한 모든 것]통증 유발하는 턱관절 장애 ‘보톡스’ 특징과 주의점
[치과에 대한 모든 것]통증 유발하는 턱관절 장애 ‘보톡스’ 특징과 주의점






