김영신 medicalkorea1@daum.net
메디톡스코리아가 2022년 출시를 목표로 차세대 보툴리눔 톡신 제제의 임상 3상에 돌입한다.
메디톡스 계열사 메디톡스코리아(대표 양기혁)는 메디톡스가 연구개발(R&D) 역량을 총 집결해 개발한 차세대 보툴리눔 톡신 제제 ‘MBA-P01’의 임상 3상 시험계획(IND)을 지난 23일 식품의약품안전처(MFDS)로부터 승인 받았다고 24일 밝혔다.
이번 승인에 따라 메디톡스코리아는 국내 4개 의료기관에서 총 318명의 중등증 및 중증의 미간 주름 개선이 필요한 환자를 대상으로 3상 임상을 한다는 계획이며, 내년 출시를 목표로 하고 있다.
‘MBA-P01’은 동결 건조 제형의 기존 보툴리눔 톡신 제제와 달리 새로운 제조공정을 적용한 원액을 사용하고 최신 기술을 적용, 생산 수율과 품질을 향상시켰다는 설명이다.
또 제조과정 중 보툴리눔 균주 배양 단계에서 사용되는 동물 유래 물질 단백질 대신 비동물성 원료 배지를 사용한 것이 특징이다.
메디톡스코리아 관계자는 “차세대 보툴리눔 톡신 제제인 ‘MBA-P01’은 보다 향상된 품질로 톡신 시장을 재편할 수 있는 무한한 잠재력을 가진 의약품이다”며, “임상 3상을 차질 없이 진행해 내년 출시 목표를 달성하고, 해외 진출을 위한 기술 수출(라이선스 아웃)등의 논의도 함께 진행할 것이다”고 말했다.
또 “보툴리눔 톡신 제제 분야에서 오랜 기간 동안 쌓아온 노하우를 바탕으로 차별화된 마케팅과 공격적인 영업 활동을 펼쳐 톡신 시장의 최강자가 메디톡스임을 입증하겠다”고 강조했다.
한편 ‘MBA-P01’은 약 20년 이상 동안 톡신 제제 분야를 연구해온 메디톡스의 R&D 역량이 총 집결된 차세대 보툴리눔 톡신 제제다. 지난 2016년 개발에 착수, 2018년부터 관련 임상을 진행했으며 이번 식약처 승인으로 임상 3상에 돌입하게 됐다.
[메디컬월드뉴스 김영신 기자]
- TAG



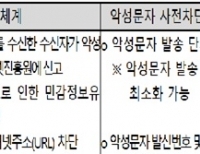 악성문자 사전차단 서비스 시범 운영
악성문자 사전차단 서비스 시범 운영
 [성형외과 시술 제대로 알기] 뒤트임 복원 및 밑트임 복원 시 고려해야 할 주의사항은?
[성형외과 시술 제대로 알기] 뒤트임 복원 및 밑트임 복원 시 고려해야 할 주의사항은?






