мһ„мһ¬кҙҖ newsmedical@daum.net
мӢқн’Ҳмқҳм•Ҫн’Ҳм•Ҳм „мІҳ(мІҳмһҘ лҘҳмҳҒ진)к°Җ мқҳм•Ҫн’Ҳ н’ҲлӘ© н—Ҳк°ҖВ·мӢ кі лҘј к°ұмӢ н•ҳкё° мң„н•ҙ м ңм¶ңн•ҙм•ј н•ҳлҠ” мҷёкөӯмӮ¬мҡ©нҳ„нҷ©м—җ лҢҖн•ң кІҖнҶ кё°мӨҖ мӢ м„Ө л“ұмқҳ лӮҙмҡ©мқ„ лӢҙмқҖ вҖҳмқҳм•Ҫн’Ҳ н—Ҳк°ҖВ·мӢ кі к°ұмӢ м§Ҳмқҳмқ‘лӢө집вҖҷмқ„ к°ңм •‧л°°нҸ¬н–ҲлӢӨкі л°қнҳ”лӢӨ.
мЈјмҡ” к°ңм • лӮҙмҡ©мқҖ в–Ін—Ҳк°ҖВ·мӢ кі к°ұмӢ нҶөліҙ нӣ„ мң нҡЁкё°к°„ л¶Җм—¬ в–Ім•Ҳм „м„ұм •ліҙ, мҷёкөӯ мӮ¬мҡ©нҳ„нҷ© л“ұ к·ңм • к°ңм •мӮ¬н•ӯ л°ҳмҳҒ в–Ім§Җл°©мІӯ м—…л¬ҙмң„мһ„ л°ҳмҳҒ л“ұмқҙлӢӨ.
мҳ¬н•ҙ мқҳм•Ҫн’Ҳ к°ұмӢ м ңлҸ„мқҳ ліёкІ©м Ғмқё мӢңн–үм—җ м•һм„ң м§ҖлӮң 2017л…„ 5мӣ” вҖҳмқҳм•Ҫн’Ҳ н—Ҳк°ҖВ·мӢ кі к°ұмӢ м§Ҳмқҳмқ‘лӢө집вҖҷмқ„ л°ңк°„н–Ҳмңјл©°, н•ҙлӢ№ м§Ҳмқҳмқ‘лӢө집мқҖ к°ұмӢ лҢҖмғҒ, к°ұмӢ мӢ мІӯ, мң нҡЁ кё°к°„, м ңм¶ң мһҗлЈҢ, н–үм •мӮ¬н•ӯ л“ұ 5к°ң 분야лЎң кө¬м„ұн–ҲлӢӨ.
мӢқм•ҪмІҳ мқҳм•Ҫн’Ҳм•Ҳм „көӯ мқҳм•Ҫн’ҲкҙҖлҰ¬кіјлҠ” вҖңмқҙлІҲ к°ңм •мқ„ нҶөн•ҙ лҜјмӣҗмқёл“Өмқҙ мқҳм•Ҫн’Ҳ н—Ҳк°Җ‧мӢ кі к°ұмӢ м ңлҸ„м—җ лҢҖн•ң мқҙн•ҙлҸ„лҘј лҶ’мһ„кіј лҸҷмӢңм—җ н–үм •м—…л¬ҙ мқјкҙҖм„ұмқ„ к°•нҷ”н•ҳлҠ”лҚ° лҸ„мӣҖмқҙ лҗ кІғмқҙлӢӨвҖқкі л°қнҳ”лӢӨ.
н•ңнҺё мһҗм„ён•ң мӮ¬н•ӯмқҖ (мӢқм•ҪмІҳ нҷҲнҺҳмқҙм§Җ) вҶ’ лІ•л №/мһҗлЈҢ вҶ’ кіөл¬ҙмӣҗм§Җм№Ём„ң/лҜјмӣҗмқём•ҲлӮҙм„ңм—җм„ң нҷ•мқён• мҲҳ мһҲлӢӨ.



 [м№ҳкіјм—җ лҢҖн•ң лӘЁл“ кІғ]мқјл°ҳм Ғ м№ҳм•„көҗм •кіј лҜёлӢҲкөҗм •мқҳ м°Ёмқҙм җкіј нҠ№м§•мқҖ?
[м№ҳкіјм—җ лҢҖн•ң лӘЁл“ кІғ]мқјл°ҳм Ғ м№ҳм•„көҗм •кіј лҜёлӢҲкөҗм •мқҳ м°Ёмқҙм җкіј нҠ№м§•мқҖ?
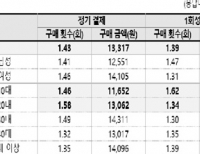 м•ұ к°ңл°ңмһҗ "мқём•ұкІ°м ң к°ҖмһҘ нҒ° л¬ём ңлҠ” кіјлҸ„н•ң мҲҳмҲҳлЈҢ"
м•ұ к°ңл°ңмһҗ "мқём•ұкІ°м ң к°ҖмһҘ нҒ° л¬ём ңлҠ” кіјлҸ„н•ң мҲҳмҲҳлЈҢ"
 [м„ұнҳ•мҷёкіј мӢңмҲ м ңлҢҖлЎң м•Ңкё°]л…ёнҷ”лЎң мқён•ң м–јкөҙ мІҳм§җ к°ңм„ вҖҳм•Ҳл©ҙкұ°мғҒмҲ вҖҷ нҠ№м§•кіј мЈјмқҳн• м җмқҖ?
[м„ұнҳ•мҷёкіј мӢңмҲ м ңлҢҖлЎң м•Ңкё°]л…ёнҷ”лЎң мқён•ң м–јкөҙ мІҳм§җ к°ңм„ вҖҳм•Ҳл©ҙкұ°мғҒмҲ вҖҷ нҠ№м§•кіј мЈјмқҳн• м җмқҖ?
 5мӣ” 1мқјл¶Җн„° лі‘м—ӯлҜён•„мһҗ лӘЁл‘җм—җкІҢ '10л…„ ліөмҲҳм—¬к¶Ң л°ңкёү'
5мӣ” 1мқјл¶Җн„° лі‘м—ӯлҜён•„мһҗ лӘЁл‘җм—җкІҢ '10л…„ ліөмҲҳм—¬к¶Ң л°ңкёү'






