애브비 스카이리치(성분명: 리산키주맙)가 세쿠키누맙 대비 52주차에 피부 개선 비율에 우월성을 보이는 최신 3b상 직접비교 임상연구 데이터가 발표됐다.
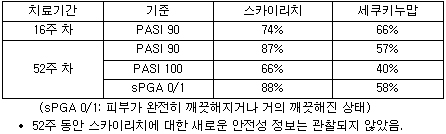
이 데이터에 따르면 스카이리치로 치료 받은 건선 환자의 66%가 52주차에 완전히 깨끗한 피부(PASI100)를 달성한 반면, 세쿠키누맙의 경우는 40%가 달성됐다(p<0.001).<br>이같은 IMMerge 3b상 오픈 라벨 연구의 새로운 직접비교 임상연구 결과는 지난 12일 진행된 미국피부과학회(AAD) 온라인 연례학술대회에서 발표됐다.
◆워렌 교수 “이번 데이터는 중요한 의미를 갖는다”
맨체스터대학교 살포드 로얄 국립의료원 재단병원 피부과센터 수석연구원이자 의학박사인 리차드 B. 워렌(RichardB. Warren) 교수는 “피부가 완전히 깨끗해지고 이를 유지하는 것이 건선 환자들의 삶에 놀라울 정도로 긍정적인 변화를 가져올 수 있는 것을 직접 확인했다”며, “현실적인 치료 목표는 완전히 깨끗한 피부라고 강조하는 건선 환자들의 의견을 고려해 볼 때, 이번 데이터는 중요한 의미를 갖는다”고 설명했다
실제 스카이리치는 세쿠키누맙 대비해 PASI 90 환자비율에서 16주차에 비열등성과 52주차에 우월성을 입증해 1차 평가변수를 충족했다.
16주차에 세쿠키누맙 치료군은 66%가 PASI 90을 달성한 반면, 스카이리치 치료군에서는 74%에서 PASI 90을 달성했다.
52주 차에는 스카이리치로 치료받은 환자 중 87%가 PASI 90을 달성한 반면, 세쿠키누맙 치료군의 경우는 57%가 PASI 90을 달성했다(p<0.001).<br>또 스카이리치로 치료받은 환자들이 세쿠키누맙으로 치료 환자와 비교했을 때 유의미하게 더 높은 비율에서 52주차에 피부가 완전히 깨끗해지거나 거의 깨끗해진 상태(sPGA 0/1)에 도달했다는 결과도 발표됐다(각각 88%, 58%, p<0.001).</p>
◆중대한 이상반응 발생률…스카이리치 치료군 5.5% vs 세쿠키누맙 치료군 3.7%
현재 유효한 안전성 정보에 따르면 52주간 새로 관찰된 안전성 정보는 없으며, 이전에 보고된 연구에서 나온 스카이리치 안전성 프로파일과 일관됐다.
이상반응 발생률은 스카이리치와 세쿠키누맙에서 비슷했다. 가장 흔한 이상반응은 비인두염, 상기도 감염, 두통, 관절통 및 설사였다.
중대한 이상반응 발생률은 스카이리치 치료군 5.5%, 세쿠키누맙 치료군 3.7%였다. 이상반응으로 투약을 중단한 비율은 스카이리치 치료군 1.2%였고 세쿠키누맙 치료군에서 4.9%였다. 두 투여군 모두에서 사망 사례는 없었다.
스카이리치는 베링거인겔하임과 애브비가 협력해 생산하는 제품으로 애브비가 개발과 글로벌 판매를 담당하고 있다.
표. 16주, 52주차 PASI90/100, sPGA0/1 에 도달한 환자비율(스카이리치 & 세쿠키누맙)
한편 애브비는 지난 1월 이 연구의 중요 결과를 발표한 바 있다.
◆IMMerge 연구는?
IMMerge는 제3b상 다기관, 무작위 배정, 오픈 라벨(두 개의 실험군), 유효성 평가자-눈가림, 활성 대조군 임상시험으로, 중등도에서 중증의 판상 건선 성인 환자를 대상으로 세쿠키누맙 대비 스카이리치의 안전성과 유효성을 평가하기 위해 설계됐다.
환자들은 베이스라인에서 투여 시작 4주 후 및 그 후 12주마다 피하 주사로 75 mg 2개(150mg)를 투여 받는 스카이리치 치료군 (n=164)과 첫 회 투여 후 1, 2, 3, 4주차 및 그 후 4주마다 피하주사로 150 mg 2개(300mg)를 투여 받은 세쿠키누맙 (n=163) 치료군에 1:1로 무작위 배정됐다.
임상시험에서는 두 가지 1차 평가변수(16주 차의 비열등성, 52주 차 우월성, 모두 PASI 90기준)와 순위화 된 세 가지 2차 평가변수(52주차 PASI 100, sPGA 0/1과 PASI 75)를 평가했다. 안전성은 모든 환자를 대상으로 평가됐다.
이 임상 연구에 대한 보다 자세한 내용은(바로가기:NCT03478787))에서 확인할 수 있다.
[메디컬월드뉴스 김영신 기자]