식품의약품안전처(처장 류영진) 식품의약품안전평가원이 발사르탄 등 사르탄류 고혈압약의 불순물 관리를 위해 ‘N-니트로소디에틸아민(NDEA)’ 잠정관리기준을 설정해 시험법을 공개했다.
안전평가원은 지난 8월과 10월 발사르탄 및 발사르탄과 구조가 유사한 사르탄류(로사르탄, 올메사르탄, 이르베사르탄, 칸데사르탄, 피마사르탄)에 대한 NDMA 잠정기준 설정 및 시험법을 공개한바 있다.
식약처가 설정한 NDEA 기준은 국제의약품규제조화위원회(ICH)가 권고하는 가이드라인(ICH M7: 의약품 중 유전독성 불순물의 평가 및 관리 가이드라인)과 외국 규제당국과의 논의를 거쳐 설정했으며, 중앙약사심의위원회의 자문을 통해 확정했다.
중앙약사심의위원회에서는 “유럽의약품안전청(EMA)과 일본후생노동성(MHLW) 등 해외 규제기관에서도 NDMA와 NDEA에 대해 1일 섭취허용량을 동일하게 설정하고 있는 점 등을 감안할 때 잠정관리기준 설정은 타당하다”고 자문했다.
식약처는 이에 앞서 업체 및 시험분석기관에서 보다 편리하고 신속하게 사르탄 계열 의약품에서 NDMA와 NDEA을 동시에 분석할 수 있는 시험법을 개발해 홈페이지에 공개했다.
이 시험법은 사르탄류 6종의 원료 및 완제의약품을 대상으로 질량분석기(LC-MS/MS)를 이용한 방법이다.
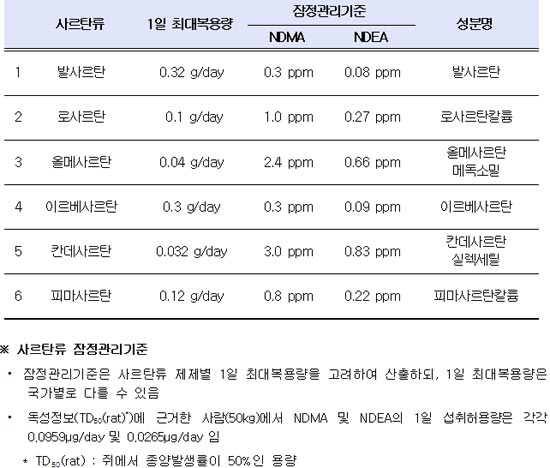
(표)사르탄류 6종 원료 및 완제의약품 중 NDMA, NDEA 잠정관리기준
[메디컬월드뉴스]