식품의약품안전처(처장 오유경)가 ‘2023년 의약품 안전성 정보 종합 보고서(제3호)’(이하 종합 보고서)를 발간한다.
이번 종합 보고서에는 ▲시판 후 안전관리 관련 법령 제‧개정 사항 ▲의약품 안전조치 사례(서한 배포 및 허가사항 변경명령) ▲의약품 안전 사용 서비스(DUR) 변경 현황 등 지난해 식약처가 조치한 의약품 안전 관련 내용 전반을 담았다.
종합 보고서에는 지난해 변경된 사항을 쉽게 찾아볼 수 있도록 종전 총리령에서 식약처 공고로 개정된 ‘의약품등 이상사례·약물이상반응 보고 서식’과 ‘공중보건 위기대응 의료제품의 안전사용 조치 및 부작용 보고 등에 관한 규칙’(총리령) 제정(안) 등 관련 법령 정보를 수록했다.
아울러 국민 보건에 영향을 줄 수 있어 긴급 배포한 ‘의약품 정보 서한’ 6건(10개 성분, 331개 품목)과 신약 등의 재심사 결과를 반영하거나 제품 사용 시 주의사항 등 추가를 위해 허가사항 변경 명령한 사례 130건(5,187개 품목)의 상세 내용을 담아 성분별 안전성 정보를 참고할 수 있도록 했다.
(표)2023년도 의약품 허가사항 변경명령 상세 현황(총 130건)
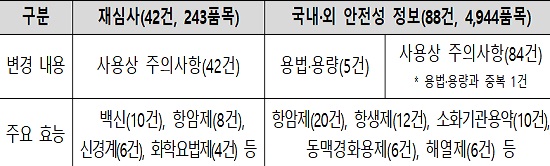
이외에도 의료현장에서 처방·조제 시 사용하는 의약품 안전 사용 서비스(DUR)의 금기 및 주의 성분 추가‧삭제 등에 지난해 변경 사항에 대한 정보를 포함하고 있다.
식약처 의약품안전국은 “이번에 종합 보고서가 업계와 의·약 전문가의 시판 후 안전관리와 약물 안전사용 등 업무에 효율적으로 활용될 것으로 기대한다.”라며, “앞으로도 국내‧외 의약품 부작용 등 정보를 적극 수집하고 규제과학 전문성을 바탕으로 신속하게 안전조치를 지속해 나가겠다.”라고 밝혔다.
한편 ‘2023년 의약품 안전성 정보 종합 보고서(제3호)’는 ‘식약처 누리집(의약품안전나라) → 안전사용 정보 → 의약품 안전성 정보 종합보고서’에서 확인할 수 있다.
[메디컬월드뉴스]