식품의약품안전처(처장 류영진) 식품의약품안전평가원이 바이오시밀러 정의, 개발과정 등을 영문으로 안내하는 ‘바이오시밀러’ 정보방을 식약처 영문 홈페이지에 개설했다고 밝혔다.
이번 정보는 우리나라 바이오시밀러 제품의 우수성을 알려 제약사 등의 수출을 지원하기 위해 마련됐다.
주요 내용은 ▲바이오시밀러의 정의 ▲바이오시밀러의 개발 과정 ▲바이오시밀러 국내 허가·심사 체계 및 허가현황 ▲바이오시밀러 영문 허가·심사 결과 등이다.
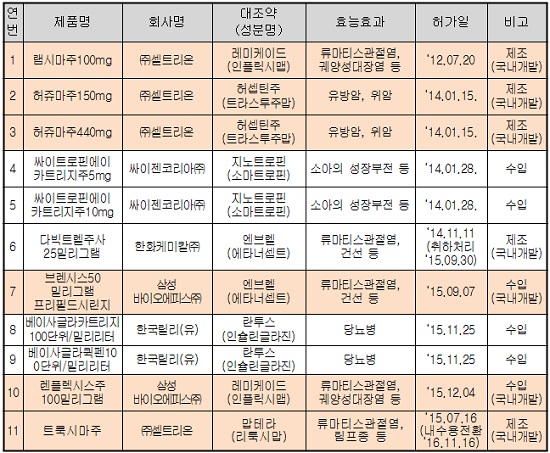
특히 식약처의 바이오시밀러에 대한 허가·심사기준으로 동등생물의약품 평가 가이드라인과 국내 개발 6개 제품을 포함하여 총 11개 제품의 바이오시밀러 허가현황도 영문으로 제공된다.
식약처는 “이번 정보방 개설을 통해 국내 개발 제품에 대한 해외에서 인지도를 높이는데 도움이 될 것”이라며, “앞으로도 국내 제약사 등이 전세계적으로 점차 커지고 있는 바이오시밀러 시장으로의 진출을 적극적으로 지원해 나가겠다”고 밝혔다.
자세한 내용은 식약처 홈페이지(
www.mfds.go.kr)→ English → Bio & Cosmetics → Biosimilar 에서 확인할 수 있다.
(표)국내 바이오시밀러 허가 현황