애브비가 범 유전자형 임상시험약물 글레카프레비르/피브렌타스비르로 모든 주요 유전자형 만성 C형 간염 환자를 8주 치료 연구에서 높은 지속 바이러스 반응율을 달성했다고 발표했다.
간경변증이 없고 치료 경험이 없는 유전자형 1형-6형 만성 C형 간염 환자 700명 이상이 참여한 연구에서, 연구 초기의 바이러스 수치와 상관 없이 치료 종료 후 12주째 지속 바이러스 반응율(SVR12)에 97.5% (n=693명/711명)도달했다. 바이러스학적 치료 실패는 1퍼센트였다(n=9/711).
이 데이터는 애브비의 글레카프레비르/피브렌타스비르 임상 개발 프로그램 내 등록 연구 중 처음 발표된 것이다.
이 임상 개발 프로그램은 기존의 미충족 수요가 있는 분야의 문제를 해결하려는 목적으로, 모든 주요 유전자형 (유전자형 1형-6형) C형 간염의 바이러스적 완치에 보다 빠르게 도달하는 방법을 찾기 위해 설계되었다.
애브비의 연구개발 부사장 겸 기업연구개발 분야 최고 책임자 마이클 세베리노(Michael Severino) 박사는 “애브비가 발표한 연구 결과는 간경변증이 없고 치료 경험이 없는 환자에게 8주간 1일1회 투여, 범 유전자형 치료제 제공에 보다 가까이 다가갔음을 보여준다. 이번 등록 연구 프로그램이 거의 완료되고 있어, 애브비의 차세대 범 유전자형 요법의 승인 신청이 미국의 규제 당국에는 연말까지, 그리고 유럽 연합과 일본에는 2017년 초까지 계획대로 제출할 수 있을 것이다”고 말했다.
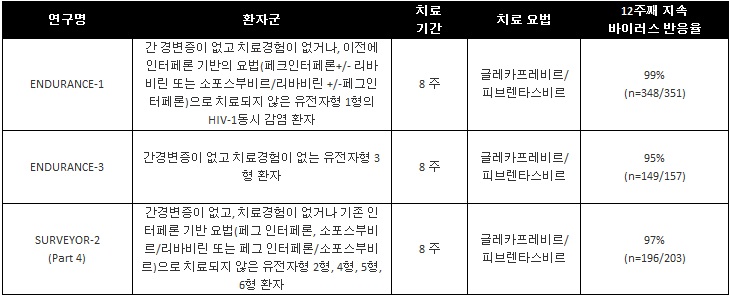
이번 새로운 중요 데이터는 글레카프레비르/피브렌타스비르의 유효성 및 안전성을 평가하는 세 가지 등록 임상시험 8주 치료군에서 얻은 결과이다.
ENDURANCE-1, ENDURANCE-3과 SURVEYOR-2 (Part 4), 이 세 개 연구의 8주 치료군 전체에서 이상 반응으로 인한 치료 중단은 없었다. 치료군 전체에서 10퍼센트 이상의 비율로 가장 흔히 나타난 이상 반응은 두통과 피로감이었다.
어떤 치료군에서도 20퍼센트 이상으로 나타난 이상 반응은 없었다. 아미노 전이효소(ALT)를 포함 임상적으로 관련성 있는 혈액검사상 이상은 관찰되지 않았다.
독일 프랑크푸르트 J.W. 괴테대학병원의 의학과장인, 책임연구자 스테판 제우젬(Stefan Zeuzem )은 “C형 간염 환자의 경우, 치료 경험이 없고, 아직 간경변증으로 진행되지 않은 질병 초기인 환자가 많은 수를 차지한다. 이런 점은 고려해 볼 때, 해당 환자군의 글레카프레비르/피브렌타스비르 8주 치료 후의 지속 바이러스 반응율을 확인할 수 있는 이번 초기 임상 데이터는 특히 고무적이다”고 말했다.
세 가지 연구에서 나타난 초기 결과의 전반적인 내용은 아래와 같다.